前列腺癌诊疗一体化里程碑!远大医药TLX591-CDx国内III期临床告捷,计划今年内递交新药上市申请,核药龙头优势凸显
5月12日,远大医药(0512.HK)股价延续上周涨势,并一举创下了8.95港元的历史高点,盘中大涨20%,市值突破300亿港元,收报8.32港元,较年内低点上涨超110%。当日晚间,远大医药再公布又一创新核药的重磅研发进展,公司用于诊断前列腺癌的全球创新在研放射性核素偶联药物(RDC) TLX591-CDx (Illuccix®, gallium Ga 68 PSMA-11)中国III期临床试验已完成全部患者入组给药,并计划今年内在中国递交新药上市申请,这已是远大医药近期公布的第三项重大创新研发进展。
在上周,远大医药先后公布其自主研发的全球创新药物STC3141在中国开展的用于治疗脓毒症的II期临床研究成功达到临床终点,以及公司用于治疗前列腺癌的全球创新RDC药物TLX591 (177Lu- HuJ591)加入国际多中心III期临床试验的申请已获得国家药监局正式受理。其中,TLX591可与TLX591-CDx可形成产品组合,促进远大医药实现前列腺癌“诊疗一体化”的全面覆盖。
TLX591-CDx:精准技术助力前列腺癌诊断革新
根据公告,TLX591-CDx是一款全球创新、基于放射性核素-小分子偶联技术的靶向前列腺特异性膜抗原(PSMA)的诊断型放射性药物,适用于转移性前列腺癌及复发性前列腺癌的诊断。TLX591-CDx中的靶向剂PSMA-11能以高亲和力的方式特异性结合在前列腺癌中高表达的PSMA上,具有可内化入细胞、生物学活性稳定、体内循环半衰期短以及对肿瘤实质的渗透性好且可被非靶向组织快速清除的五大特点。
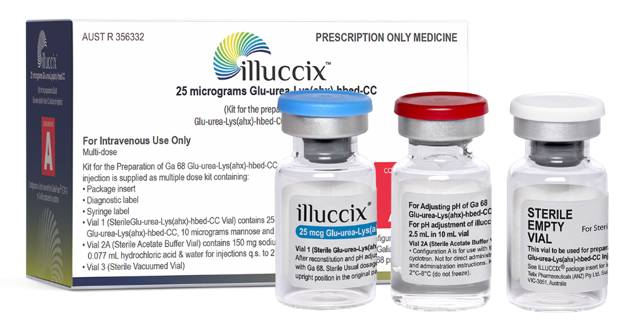
▲(图片来源:远大医药官方公众号)
TLX591-CDx在全球注册上市的工作进展顺利,该产品已在澳大利亚、美国、加拿大、巴西、英国,以及多个欧洲国家获批上市,于2024年实现近5.17亿美元的销售额,并于今年第一季度取得近1.51亿美元的销售额,同比增长近35%。
本次完成全部入组的是一项单臂、开放标签的III期临床研究,拟在超过100例经前列腺癌根治术和/或根治性放疗后生化复发患者中使用TLX591-CDx并进行正电子发射断层成像/计算机断层扫描(PET/CT)或正电子发射断层成像/磁共振成像(PET/MRI)检测,以评估产品的诊断有效性,同时评估产品在中国人群中的安全性和耐受性。本次临床的顺利推进将进一步加速该产品在中国的上市进程,并为远大医药实现前列腺癌“诊疗一体化”奠定坚实的基础。
另一方面,远大医药用于治疗前列腺癌的RDC产品TLX591加入国际多中心III期临床试验的申请早前已获得国家药监局受理。据悉,TLX591凭借其精准靶向特性和差异化药理学优势,已展现出超越现有抗前列腺特异性膜抗原(PSMA)小肽靶向放射性配体治疗(RLT)分子的临床潜力,有望重新定义PSMA阳性的转移性去势抵抗性前列腺癌(mCRPC)的治疗标准。未来,随着该临床研究积极推进,,上述两款产品组合正蓄势待发,有望为中国前列腺疾病患者带来更为精准、高效的诊疗方案。
创新驱动显成效,全球化布局彰显核药领军地位
核药抗肿瘤诊疗是远大医药重点布局的战略领域之一,公司围绕肿瘤诊疗一体化的治疗理念,在该领域的研发注册阶段储备了15款创新产品,涵盖68Ga、177Lu、131I、90Y、89Zr在内的5种放射性核素,覆盖了肝癌、前列腺癌、肾癌、脑癌等在内的7个癌种;产品种类兼具诊断和治疗,可为患者提供多适应症治疗选择、多手段且诊疗一体化的全球领先的抗肿瘤方案。
目前,远大医药在核药抗肿瘤诊疗板块已有4款RDC创新药获批开展注册性临床研究,其中3款已进入III期临床阶段:用于诊断前列腺癌的在研产品TLX591-CDx已于近日完成全部患者入组;诊断肾透明细胞癌产品TLX250-CDx已于2024年11月完成首例患者入组给药;以及治疗胃肠胰腺神经内分泌瘤的产品ITM-11已于2025年3月完成国际多中心COMPOSE试验的中国首例患者入组给药。此外,公司全球创新、基于放射性核素-抗体偶联技术的靶向磷脂酰肌醇蛋白聚糖3 (GPC-3)的诊断型放射性药物GPN02006早前在中国开展的研究者发起的临床研究(IIT临床研究)取得了里程碑式突破,临床研究数据表明,GPN02006展现出卓越的安全性和显像效能:所有受试者给药后均未报告任何药物相关不良反应,安全耐受性表现优异;给药后30分钟即可实现高质量显像,充分满足肝细胞癌临床快速诊断需求。GPN02006产品极具潜力,有望成为全球首个针对GPC-3靶点的HCC诊断类RDC产品。
目前,远大医药是拥有进入中国III期临床研究中诊断和治疗类RDC创新药总计储备最多的企业,也是全球范围内在核药抗肿瘤领域拥有最丰富产品管线和诊疗一体化布局的创新药企之一,是名副其实的全球核药领军企业,且是全球仅有的四家在肿瘤治疗方面成功实现创新核药商业化应用的创新制药企业之一——远大医药核药板块核心产品易甘泰®钇[90Y]微球注射液已经成为业绩增长的核心引擎,该产品于2024年贡献收入近5亿港元,同比增速超140%,连续两年实现销售收入的同比超过100%的大幅上涨,并推动公司核药板块实现收入近177%的大幅增长。
在产业布局方面,远大医药已实现了研发、生产、销售、监管资质等多个环节的全方位布局,建立了完整的产业链。同时,公司位于成都温江的放射性药物全球研发及生产基地早前已完成主体结构封顶,并已于今年3月完成生态环境部组织的辐射安全许可证现场检查。
据悉,远大医药成都核药基地定位于全球创新核药产业化高地,聚焦同位素工艺开发与制备、核药偶联技术、自动化标记技术等核心领域,覆盖核药早研、工艺开发、质控、非临床研究、智能生产与精准配送一站式全生命周期管理,树立世界一流研发生产质量与运营体系。此外,该基地通过全流程智能监控与闭环管理,致力于建设全球首个零辐射智能核药工厂,是目前国际范围内核素种类最全、自动化程度最高的智能工厂。同时,该基地也将与公司美国波士顿研发中心、远大医药-山东大学放射药物研究院等共同构建成为其全球核药研发中心网络,并依托科技创新、全球人才与智能制造,全面夯实远大医药在核药领域的领先地位。
随着成都核药基地投入使用,远大医药全球创新核药管线的落地将进入新的阶段,同时也将促进公司培育更多高价值的重磅核药品种,进一步将稳固公司核药产业的全球化领军地位。
重症治疗取得里程碑突破,创新成果获投行力挺
除了核药领域,远大医药上周亦公布了其在危重症治疗领域的重磅进展,公司自主研发的全球创新药物STC3141继中国II期临床成功达到临床终点。优异的临床结果证实了STC3141在脓毒症治疗中的有效性和安全性,为重症治疗领域带来新的突破,并有望推动脓毒症治疗迈入一个新纪元。
据悉,STC3141是由远大医药自主开发的、拥有全球知识产权的、具有全新作用机制的小分子化合物,其通过中和胞外组蛋白和中性粒细胞诱捕网来逆转机体过度免疫反应造成的器官损伤,可用于脓毒症等多种重症适应症。该产品相关研究结果已发布于顶级学术期刊《Nature Communications》和《Critical Care》,具有深远的学术影响力。
STC3141是全球首个以重新构建免疫稳态为核心的脓毒症治疗方案,实现了治疗维度的重大升级,在现有的抗感染、液体复苏和维持器官运转等对症支持治疗的基础上,针对机体免疫失调这个核心病因加以精准调节,帮助身体恢复平衡,填补了当前脓毒症针对病因治疗的临床空白。
尽管医学技术不断进步,脓毒症的发病率和病死率仍然居高不下。全球范围内每年新发脓毒症约4,900万例,超1/5的患者死亡,约占全球总死亡人数的20%。国内重症监护病房的脓毒症发生率为20.6%~50.8%,约1/3的患者发生院内死亡。在高收入国家,脓毒症患者的全院平均治疗费用超过3.2万美元。Wise Guy Reports数据显示,2024年全球脓毒症治疗药物市场规模为125.4亿美元,预计到2032年市场规模将达到193.7亿美元,年均复合增长率为5.58%。

▲(图源:Wise Guy Reports)
随着STC3141的顺利开发,其未来有望打破脓毒症领域长期缺乏针对性药物的困境,成为重症治疗领域首个具有开创性意义的突破性疗法,精准响应并满足临床治疗的迫切需求。
近期以来,远大医药多个领域创新研发进展频频,公司前瞻性创新布局优势凸显,而陆续取得的硕果不仅受到了市场的广泛认可,同时也获得了多家投行及券商的力挺。
中金公司早前发布研报指出,维持远大医药跑赢行业评级(即未来6-12个月公司个股表现预计将超过同期其所属的中金公司行业指数),并进一步将目标价上调近11%至8.00港元。此外,华福证券也在其报告中推荐关注远大医药,报告指出,目前脓毒症患者众多、死亡率高,且患者预后不佳,新药研发困难,约1/3患者一年内死亡,远大医药STC3141的免疫稳态疗法有利于脓毒症恢复。
创新成果的陆续落地,以及资本市场的持续青睐反映了远大医药全球化创新布局的优势,以及公司杰出的创新研发实力和商业化落地能力。展望未来,远大医药的全球化战略和多元创新产品管线为其在竞争激烈的医药市场中占据有利地位提供了保障,并也将为其全球化科技创新型药企的前进之路持续赋能,助力公司再创新的高峰。
-
捷迈邦美发布最新财报,全球龙头要放弃传统骨科业务?
2025-05-09 15:00:18
-
全球首个零辐射核药研发生产基地蓄势待发,远大医药创新产品管线夯实核药国际领军地位
2025-05-08 08:57:39
-
大裁员引发巨震!美国19州起诉小肯尼迪
2025-05-07 18:47:28
MedTrend
∣ 医趋势
医疗前沿资讯 | 趋势观察洞见 | 组织与领导力 | 人才解决方案


长按,识别二维码,加关注
